Auteurs:
Pier-Luc Laporte, technologiste médical et Philippe Desmeules, Ph.D, DEPD, CSPQ, Biochimiste clinique; Grappe Capitale Nationale et des Îles de la Madeleine, Site Institut Universitaire de Cardiologie et de Pneumologie de Québec, Québec, Qc.
Commentaire de Philippe Desmeules, responsable de la section Normes, Analytique et Technologie :
Cet article est présenté afin de mettre en évidence la réalité du laboratoire et son impact dans certaines circonstances lors de l’utilisation adéquate d’un appareil automatisé. Parfois, le contexte clinique peut pousser à utiliser un appareil dans de mauvaises conditions analytiques et ceci à l’insu de l’utilisateur puisque rien n’est alors révélé ou mis en évidence par l’appareillage (i.e. absence d’un code d’erreur).
Souvent la réalité en laboratoire (i.e. appels en provenance des unités, pression de l’urgence, inexpérience, mauvaise interprétation du contexte analytique, possibilité de faire l’action ou non d’une façon automatisée) pousse le laborantin à s’aventurer dans des zones risquées. Dans la littérature, le secteur à haut débit de la biochimie est souvent présenté comme un service pratiquement exempt de possibilités d’erreurs analytiques. C’est vrai, les erreurs analytiques se font de plus en plus rares. Toutefois lorsqu’une erreur analytique survient elle s’explique majoritairement par l’interface humain-automate qui n’a pas bien communiqué!
Introduction
En pleine nuit, une patiente de l’urgence fortement suspectée de souffrir d’une intoxication à l’acétaminophène est prélevée afin d’obtenir un dosage de l’acétaminophène plasmatique. Le résultat s’avère négatif et le résultat indiqué par le laboratoire est alors de < 13,2 µmol/L. Dans les instants suivant l’émission du résultat, un membre du personnel de l’urgence téléphone au technologiste du laboratoire de biochimie. Cette personne émet alors sa grande réserve sur la véracité du résultat car, selon elle et le médecin, l’échantillon sanguin de la patiente devrait contenir de l’acétaminophène puisque l’histoire clinique de la patiente indique une consommation excessive presque certaine d’acétaminophène dans les moments précédant son arrivée à l’urgence.
Cherchant à offrir le meilleur service possible, le technologiste se pose alors la question : « est-ce possible que la concentration soit tellement élevée que l’appareil indique erronément une concentration sous le seuil de la sensibilité? » Une dilution automatisée est alors demandée sur le même échantillon directement à l’écran de l’appareil.
Le multi-analyseur intégré Siemens Vista 1500 permet la dilution automatisée d’un tel résultat (< 13,2 µmol/L), même s’il est sous le domaine de mesure et sans code d’erreur. Le résultat obtenu après la dilution automatisée est alors de 126 µmol/L et il n’est pas accompagné d’un code d’erreur. L’urgence est alors informée qu’un rapport corrigé sera produit afin d’indiquer que l’échantillon contenait effectivement de l’acétaminophène mais étonnamment pas en concentration toxique. Le lendemain, cette situation a été rapportée au coordonnateur technique et au biochimiste clinique de garde. De plus, une non-conformité avait été déclarée dans le système de gestion des non-conformités (Wehoop, Kiwi technologies). Une enquête a alors été réalisée pour bien comprendre ce qui a causé ce changement de résultat plutôt surprenant à la suite d’une dilution sur un échantillon ne contenant pas d’acétaminophène.
Enquête
1- Éléments analytiques à connaître
Afin de bien comprendre la démarche présentée, voici quelques informations à garder en tête. La solution (diluant) utilisée par l’appareil pour diluer automatiquement l’échantillon est de l’eau désionisée. L’appareil Vista 1500 désionise l’eau via un système de purification intégré à l’appareil. Cette eau présente une résistivité élevée qui est habituellement de 17 MΩ-cm. Cette eau purifiée est utilisée pour diluer les échantillons pour le dosage de l’acétaminophène et aussi pour d’autres analyses.
Le domaine de mesure de l’acétaminophène s’étend de 13,2 à 1985,4 µmol/L. La dilution automatique est disponible en toutes circonstances, c’est-à-dire même si l’échantillon contient une quantité non détectable d’acétaminophène (<13,2 µmol/L). L’appareil permet de déclencher une dilution de facteur 2 avec l’eau déionisée comme diluant. Il faut toutefois noter que pour faire une dilution plus marquée (et donc manuelle), la compagnie suggère d’utiliser l’étalon DRUG2 std (0 µmol/L) qui est habituellement utilisé pour étalonner les analyses de médicaments. Il est aussi possible d’utiliser le plasma d’un patient qui ne contient pas d’acétaminophène.
Rappelons que le dosage de l’acétaminophène est un test colorimétrique à deux étalons (un étalon zéro et un étalon à 2100 µmol/l) et inversement proportionnel (pente d’absorbance négative). Cette méthode est basée sur l’hydrolyse enzymatique de l’acétaminophène produisant du p-aminophénol et de l’acétate. Le p-aminophénol est produit proportionnellement à la quantité d’acétaminophène présente en solution. La quantité de p-aminophénol produit est ensuite révélée par une réaction colorimétrique impliquant l’o-crésol et le sulfate de cuivre ammoniacal qui ultimement formeront de l’indophénol mesuré à 600 nm (point final, temps de réaction de 6,4 minutes). La figure suivante présente l’étalonnage de l’acétaminophène en termes de signal vs concentration et la courbe de corrélation.
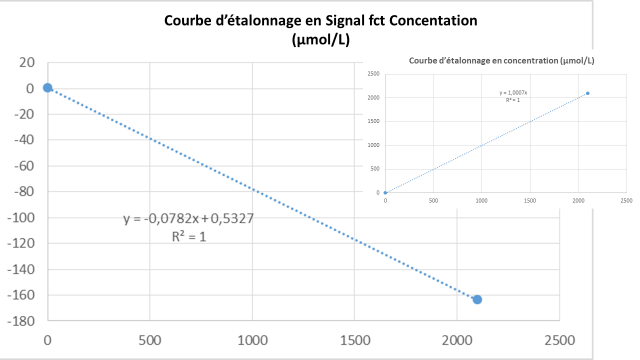
N.B : Dans tous les tableaux présentés, les cases en rouge ont été obtenues à la suite d’une procédure d’extraction à partir de la base de données de l’appareil. En fait, aucun de ces résultats ne peut s’afficher à l’écran de l’appareil, ni à l’intergiciel, ni au SIL. Ces résultats ont été extraits pour investiguer la problématique mais l’utilisateur de l’appareil n’a pas accès en routine à ces données puisqu’il est nécessaire de faire l’arrêt total de l’appareil pour y accéder.
2-Répétition du phénomène
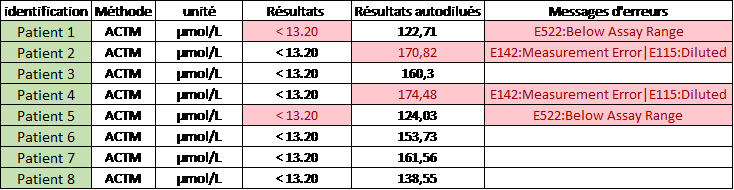
Afin de recréer l’observation rapportée, huit échantillons de patients différents ne contenant pas d’acétaminophène ont été dilués de façon automatique par l’appareil (eau désionisée du système) et sont présentés dans le tableau suivant. Six des huit patients présentaient un résultat d’acétaminophène même s’ils n’en contenaient pas. Pour deux cas seulement (résultats > 170 µmol/L), l’appareil a indiqué un code d’erreur E115 et E142. Le code E115 est un code automatique ajouté à chaque résultat ayant été dilué par l’appareil, soit de façon réflexe ou demandé par l’utilisateur. Pour ce qui est du code E142, celui-ci apparait lorsqu’un paramètre d’auto-vérification de la réaction est hors des normes établies par Siemens (i.e. absorbance trop faible au départ de l’analyse, cinétique trop rapide, etc). Il devenait alors clair que l’eau pouvait provoquer un résultat de patient erroné d’acétaminophène et que ce résultat pouvait apparaître sans code d’erreur comme dans les 6 cas sur 8.
Effet de la dilution par l’eau pour des échantillons de patients (plasma) ne contenant pas d’ACTM
3-Dilutions en série du plasma
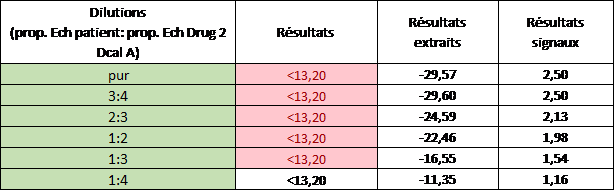
Le plasma du patient en question a été dilué en série. Il est important de noter que pour réaliser ces dilutions en série le diluant était l’étalon DRUG2 std suggéré par la compagnie pour les dilutions manuelles (donc lors d’une dilution par un facteur > 2 car la dilution automatique à bord est uniquement d’un facteur de 2).
Le tableau suivant, montre la linéarité des dilutions en utilisant l’étalon DRUG2 std (nommé aussi Drug2 Dcal A). Fait intéressant, malgré les dilutions, aucun résultat ne s’approche de la valeur produite de 126 µmol/L obtenu par dilution avec l’eau.
Linéarité des dilutions en utilisant l’étalon DRUG2 std (ou Drug 2 Dcal A)
4-Dosage de l’acétaminophène dans l’eau désionisée
Afin de prouver que l’eau s’avère l’élément perturbateur lors de cette réaction colorimétrique, un dosage d’acétaminophène a été effectué directement sur un échantillon d’eau déionisée. Dans ce cas, lorsque l’on tente une mesure sur cet échantillon complètement aqueux, on obtient un résultat erroné et accompagné d’un code d’erreur E142 informant l’utilisateur du problème.

5-Étude du comportement analytique pour des concentrations très élevées d’acétaminophène et évaluation de l’effet de la proportion d’eau dans la réaction
L’eau désionisée ayant été identifiée comme l’élément qui interfère dans la réaction du dosage colorimétrique de l’acétaminophène, une étude plus poussée a été effectuée afin de : démontrer qu’une concentration élevée ne pouvait pas produire un résultat sous le domaine de mesure (< 13,2 µmol/L) et voir à partir de quelle proportion d’eau déionisée le dosage déviait de la linéarité.
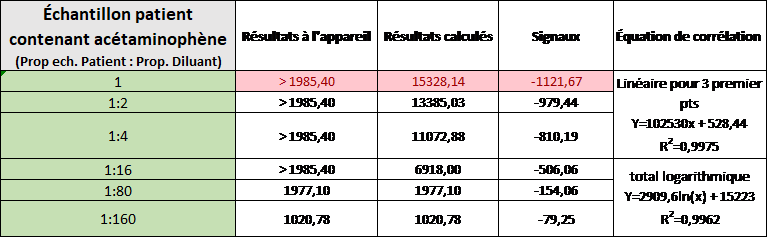
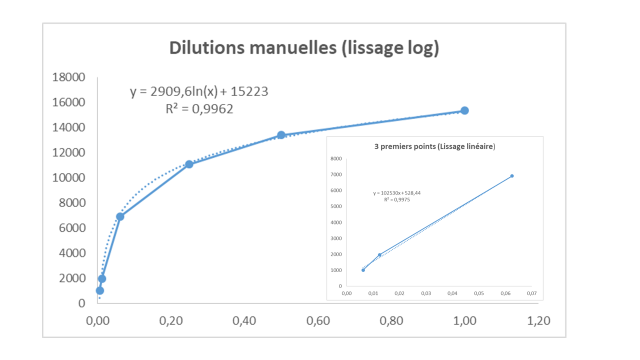
Pour ce faire, deux comprimés d’acétaminophène (350 mg) ont été broyés et solubilisés dans environ 4 mL de plasma d’un pool de patients qui ne contenait pas d’acétaminophène au départ. Cet échantillon de pool patient dopé en acétaminophène a été centrifugé et ensuite dilué jusqu’à l’obtention d’une valeur mesurable par l’appareil. Le tableau A, montre des concentrations très élevées d’acétaminophène mais aucun dosage n’a affiché le résultat < 13,2 µmol/L. Comme le démontre la figure suivante, les résultats de dilutions respectent aussi la linéarité pour les concentrations sous 2000 µmol/L. Pour les concentrations très élevées, comme pour notre pool de patient dopé initial (160 000 µmol/L), on peut remarquer que le signal est fortement saturé (voir le lissage logarithmique). À ces fortes concentrations, le signal n’est plus proportionnel à la concentration.
A) Analyses effectuées comme de routine (dilution manuelle effectuée avec un pool d’échantillon de patients négatifs en acétaminophène)
Le tableau B présente l’effet d’une dilution automatisée supplémentaire en utilisant de l’eau sur les échantillons déjà dilués manuellement avec l’étalon Drug2 std.
B) Analyses effectuées avec une dilution supplémentaire par l’appareil avec l’eau du système sur l’aliquote original conservée à bord de l’appareil
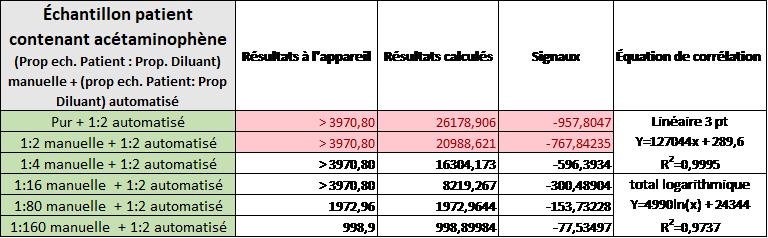
6-Linéarité de la réaction lors de dilutions avec le Drug 2 STD ou l’eau
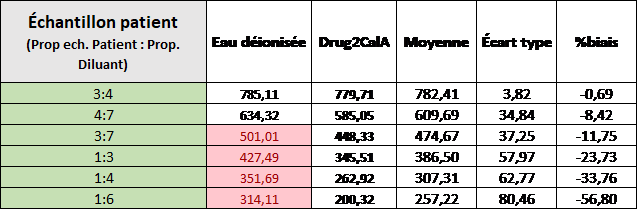
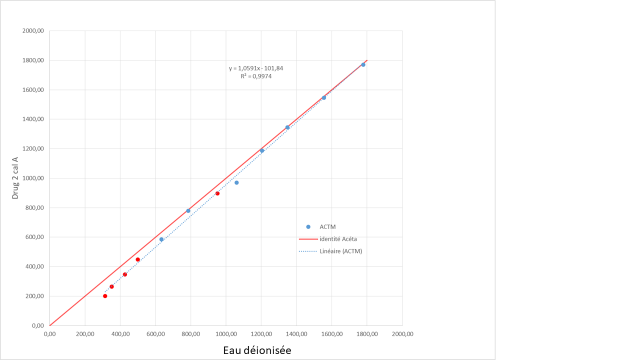
Un échantillon de patient a été dilué en série avec de l’eau ainsi qu’avec le diluant recommandé par la compagnie (Drug 2 STD A) afin de déterminer à quelle proportion d’eau l’analyse dévie de la linéarité. Comme démontré dans le tableau suivant, à une dilution de 3:7 (2,33) avec de l’eau les résultats s’éloignent (biais) de la valeur attendue et un code d’erreur apparaît (case en rouge). Du côté du diluant Drug2 std, les résultats respectent la linéarité et il n’y a pas de codes d’erreur. Le biais relatif présenté est le biais entre le résultat obtenu de la dilution Drug 2 et le résultat obtenu de la dilution avec l’eau déionisée. On peut constater que les résultats entre les deux diluants divergent très rapidement. Le graphique suivant présente la corrélation entre les résultats obtenus avec l’eau déionisée en fonction de ceux obtenus avec l’étalon Drug 2.
A) Comparaison entre les deux types de diluant
B) Courbe de corrélation
7-Validation des résultats et calculs des biais selon la valeur calculée après dilution
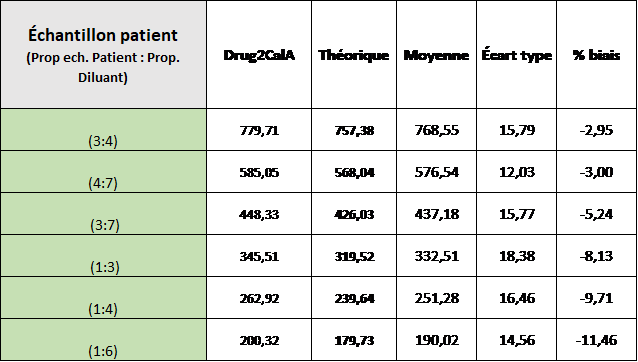
Dans cette section, les résultats obtenus pour les deux diluants ont été comparés aux valeurs attendues calculées. Cet exercice nous a permis de mettre en évidence les biais qui s’installent progressivement pour les deux diluants. Lorsque la dilution est effectuée avec l’étalon Drug2 Cal A, on obtient un biais relatif avec la valeur de dilution attendue qui s’étend de -2,95 à -11,46 %. Ces biais sont plutôt de qualité moyenne mais les résultats sont cliniquement utilisables. Toutefois, l’analyse de l’acétaminophène n’est pas une analyse qui peut être diluée parfaitement, même avec cet étalon.
A) Dosages d’acétaminophènes pour des échantillons dilués avec l’étalon Drug 2 Cal A en comparaison de la valeur calculée
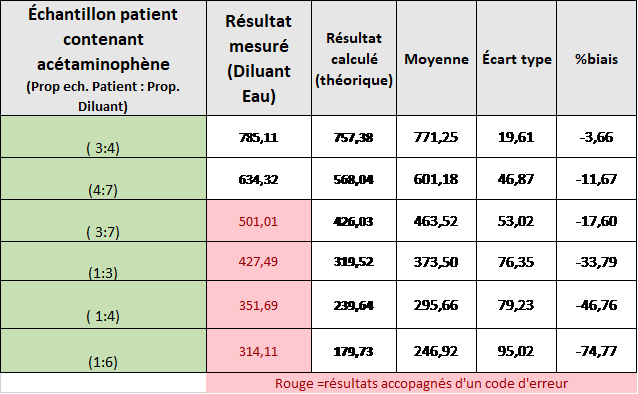
Pour la dilution avec l’eau, on peut voir que le biais qui s’installe lors des dilutions est catastrophique allant même jusqu’à -75%. L’eau n’est tout simplement pas un diluant pour cette analyse. Même lorsque la proportion d’eau est de 1,75 (4 :7), un biais de -11,67 % est déjà présent ce qui fait que la dilution permise par Siemens à bord de l’instrument (facteur de 2) n’est pas recommandée selon nous.
B) Dosages d’acétaminophène pour des échantillons dilués avec de l’eau désionisée en comparaison avec la valeur calculée après dilution
8-Conclusion
On doit conclure que même si une dilution automatisée est disponible et permise sur un appareil, elle peut ne pas être idéale ou même recommandée. Par surcroît, même si le résultat obtenu est exempt d’un code d’erreur, il peut être erroné!
Il est surprenant que le feuillet qui accompagne l’analyse ne rapporte pas le danger de diluer avec de l’eau. De plus, il serait opportun que lorsqu’un utilisateur demande une dilution automatique pour un résultat sous la sensibilité que l’appareil pose une question du genre : « voulez-vous vraiment diluer cet échantillon qui présente un résultat de < 13,2? »
Par ailleurs, une bonne pratique consisterait à faire un minimum de deux dilutions (en série par exemple) afin de s’assurer de la linéarité des résultats obtenus, surtout lors de la dilution d’un résultat sous le domaine de mesure, ce qui n’est pas pratique courante.
En résumé, l’eau désionisée est souvent un mauvais diluant pour les analyses en biochimie, sa faible force ionique et son pH acide pouvant perturber la réaction, forcer la précipitation de protéines et briser les interactions entre les enzymes et leurs ligands. Il est donc important que les dilutions avec de l’eau fassent l’objet d’une validation avant d’en autoriser l’utilisation tous azimuts!!

